ยูโรเพียมสัญลักษณ์คือ Eu และเลขอะตอมคือ 63 เนื่องจากเป็นธาตุทั่วไปของแลนทาไนด์ ยูโรเพียมจึงมีวาเลนซ์ +3 แต่พบได้ทั่วไปคือออกซิเจน +2 ยูโรเพียมมีสารประกอบที่มีสถานะวาเลนซ์ +2 น้อยกว่า เมื่อเปรียบเทียบกับโลหะหนักชนิดอื่น ยูโรเพียมไม่มีผลทางชีวภาพที่สำคัญและค่อนข้างไม่เป็นพิษ การใช้งานยูโรเพียมส่วนใหญ่ใช้เอฟเฟกต์การเรืองแสงของสารประกอบยูโรเพียม ยูโรเพียมเป็นหนึ่งในธาตุที่มีน้อยที่สุดในจักรวาล มีเพียงประมาณ 5 ชนิดในจักรวาล × 10-8% ของสารเป็นยูโรเพียม
ยูโรเพียมมีอยู่ในมอนาไซต์
การค้นพบยูโรเพียม
เรื่องราวเริ่มต้นในช่วงปลายศตวรรษที่ 19 ในเวลานั้น นักวิทยาศาสตร์ที่เก่งกาจเริ่มเติมเต็มตำแหน่งว่างที่เหลือในตารางธาตุของเมนเดเลเยฟอย่างเป็นระบบโดยการวิเคราะห์สเปกตรัมการแผ่รังสีอะตอม ในมุมมองปัจจุบัน งานนี้ไม่ใช่เรื่องยาก และนักศึกษาระดับปริญญาตรีก็สามารถทำได้ แต่ในเวลานั้น นักวิทยาศาสตร์มีเพียงเครื่องมือที่มีความแม่นยำต่ำและตัวอย่างที่ยากต่อการทำให้บริสุทธิ์ ดังนั้น ตลอดประวัติศาสตร์ของการค้นพบแลนทาไนด์ ผู้ค้นพบ "กึ่งๆ" ทั้งหมดจึงยังคงกล่าวอ้างเท็จและโต้เถียงกันเอง
ในปี พ.ศ. 2428 เซอร์วิลเลียม ครูกส์ได้ค้นพบสัญญาณแรกของธาตุที่ 63 แต่ไม่ชัดเจนนัก โดยเขาสังเกตเห็นเส้นสเปกตรัมสีแดงเฉพาะ (609 นาโนเมตร) ในตัวอย่างซาแมเรียม ระหว่างปี พ.ศ. 2435 ถึง พ.ศ. 2436 ผู้ค้นพบแกลเลียม ซาแมเรียม และดิสโพรเซียม คือ พอล เอ ไมล์ เลอโคก เดอ บัวส์โบดราน ได้ยืนยันแถบนี้และค้นพบแถบสีเขียวอีกแถบหนึ่ง (535 นาโนเมตร)
ในปี 1896 Eugène Anatole Demar ก็ได้แยกซาแมเรียมออกไซด์ด้วยความอดทน และยืนยันการค้นพบธาตุหายากชนิดใหม่ซึ่งอยู่ระหว่างซาแมเรียมและแกโดลิเนียม เขาแยกธาตุนี้ออกได้สำเร็จในปี 1901 ซึ่งถือเป็นจุดสิ้นสุดของการค้นพบครั้งนี้ “ผมหวังว่าจะตั้งชื่อธาตุใหม่นี้ว่ายูโรเพียม โดยมีสัญลักษณ์ว่า Eu และมีมวลอะตอมประมาณ 151”
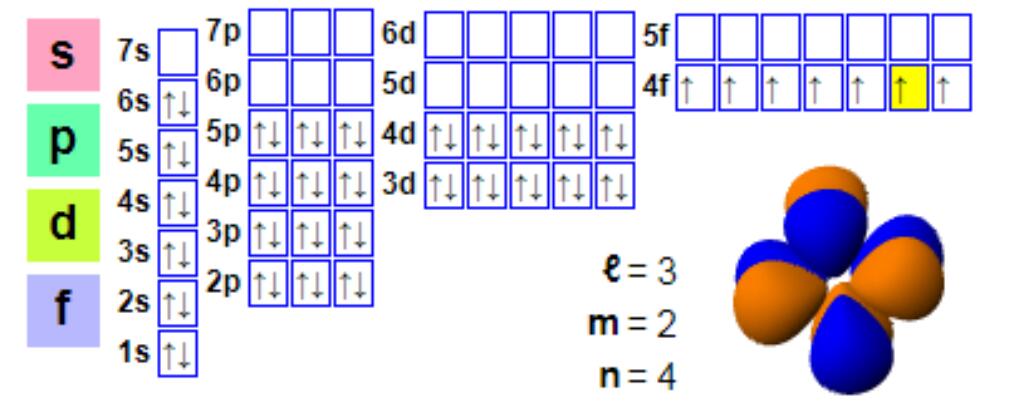
โครงสร้างอิเล็กตรอน
โครงสร้างอิเล็กตรอน:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p66s2 4f7
แม้ว่ายูโรเพียมจะมีวาเลนซ์สามชนิด แต่ก็มีแนวโน้มที่จะก่อตัวเป็นสารประกอบวาเลนซ์สองชนิด ปรากฏการณ์นี้แตกต่างจากการก่อตัวของสารประกอบวาเลนซ์ +3 โดยแลนทาไนด์ส่วนใหญ่ ยูโรเพียมวาเลนซ์สองชนิดมีการกำหนดค่าอิเล็กตรอนเป็น 4f7 เนื่องจากชั้น f ที่เติมเข้าไปครึ่งหนึ่งทำให้มีเสถียรภาพมากกว่า และยูโรเพียม (II) และแบเรียม (II) ก็มีความคล้ายคลึงกัน ยูโรเพียมวาเลนซ์สองชนิดเป็นตัวรีดิวซ์อ่อนๆ ที่ทำปฏิกิริยาออกซิไดซ์ในอากาศเพื่อสร้างสารประกอบของยูโรเพียม (III) ภายใต้สภาวะที่ไม่มีอากาศ โดยเฉพาะสภาวะการให้ความร้อน ยูโรเพียมวาเลนซ์สองชนิดจะมีเสถียรภาพเพียงพอ และมีแนวโน้มที่จะรวมเข้ากับแคลเซียมและแร่ธาตุอัลคาไลน์เอิร์ธอื่นๆ กระบวนการแลกเปลี่ยนไอออนนี้เป็นพื้นฐานของ "ความผิดปกติเชิงลบของยูโรเพียม" นั่นคือ เมื่อเทียบกับคอนไดรต์ที่มีอยู่มากมาย แร่ธาตุแลนทาไนด์หลายชนิด เช่น มอนาไซต์ จะมีปริมาณยูโรเพียมต่ำ เมื่อเปรียบเทียบกับมอนาไซต์ บาสต์เนไซต์มักแสดงค่าความผิดปกติของยูโรเพียมเชิงลบน้อยกว่า ดังนั้น บาสต์เนไซต์จึงเป็นแหล่งที่มาหลักของยูโรเพียมด้วย
ยูโรเพียมเป็นโลหะสีเทาเหล็กที่มีจุดหลอมเหลว 822°C จุดเดือด 1597°C และความหนาแน่น 5.2434 g/cm³ เป็นธาตุที่มีความหนาแน่นน้อยที่สุด อ่อนที่สุด และระเหยง่ายที่สุดในบรรดาธาตุหายาก ยูโรเพียมเป็นโลหะที่มีฤทธิ์แรงที่สุดในบรรดาธาตุหายาก โดยที่อุณหภูมิห้อง จะสูญเสียความแวววาวของโลหะในอากาศทันที และถูกออกซิไดซ์เป็นผงอย่างรวดเร็ว ทำปฏิกิริยารุนแรงกับน้ำเย็นเพื่อสร้างก๊าซไฮโดรเจน ยูโรเพียมสามารถทำปฏิกิริยากับโบรอน คาร์บอน กำมะถัน ฟอสฟอรัส ไฮโดรเจน ไนโตรเจน เป็นต้น
การประยุกต์ใช้ยูโรเพียม
ยูโรเพียมซัลเฟตเปล่งแสงเรืองแสงสีแดงภายใต้แสงอัลตราไวโอเลต
Georges Urbain นักเคมีหนุ่มผู้โดดเด่นได้สืบทอดเครื่องมือ Spectroscopy ของ Demar çay และค้นพบว่าตัวอย่างออกไซด์ Yttrium(III) ที่มีการเจือปนด้วยยูโรเพียมปล่อยแสงสีแดงที่สว่างมากในปี 1906 ซึ่งถือเป็นจุดเริ่มต้นของการเดินทางอันยาวนานของวัสดุเรืองแสงยูโรเพียมซึ่งไม่เพียงแต่ใช้ในการปล่อยแสงสีแดงเท่านั้น แต่ยังรวมถึงแสงสีน้ำเงินด้วย เนื่องจากสเปกตรัมการปล่อยของ Eu2+ อยู่ในช่วงดังกล่าว
สารเรืองแสงที่ประกอบด้วยตัวปล่อย Eu3+ สีแดง Tb3+ สีเขียว และ Eu2+ สีน้ำเงิน หรือสารผสมของสารเหล่านี้ สามารถแปลงแสงอัลตราไวโอเลตเป็นแสงที่มองเห็นได้ วัสดุเหล่านี้มีบทบาทสำคัญในเครื่องมือต่างๆ ทั่วโลก เช่น แผ่นฉายรังสีเอกซ์ หลอดรังสีแคโทด หรือแผ่นฉายพลาสมา ตลอดจนหลอดฟลูออเรสเซนต์ประหยัดพลังงานและไดโอดเปล่งแสงในปัจจุบัน
เอฟเฟกต์การเรืองแสงของยูโรเพียมไตรวาเลนต์ยังสามารถได้รับการทำให้ไวต่อแสงโดยโมเลกุลอะโรมาติกอินทรีย์ และสารเชิงซ้อนดังกล่าวสามารถนำไปใช้ในสถานการณ์ต่างๆ ที่ต้องมีความไวสูง เช่น หมึกป้องกันการปลอมแปลงและบาร์โค้ด
นับตั้งแต่ทศวรรษ 1980 ยูโรเพียมได้มีบทบาทสำคัญในการวิเคราะห์ชีวเภสัชกรรมที่มีความไวสูงโดยใช้วิธีการเรืองแสงเย็นแบบแก้ไขตามเวลา ในโรงพยาบาลและห้องปฏิบัติการทางการแพทย์ส่วนใหญ่ การวิเคราะห์ดังกล่าวได้กลายเป็นเรื่องปกติ ในการวิจัยด้านวิทยาศาสตร์ชีวภาพ รวมถึงการถ่ายภาพทางชีวภาพ หัววัดเรืองแสงทางชีวภาพที่ทำจากยูโรเพียมและแลนทาไนด์อื่นๆ มีอยู่ทั่วไป โชคดีที่ยูโรเพียม 1 กิโลกรัมเพียงพอสำหรับการวิเคราะห์ประมาณ 1 พันล้านครั้ง หลังจากที่รัฐบาลจีนได้จำกัดการส่งออกแร่ธาตุหายากเมื่อไม่นานนี้ ประเทศอุตสาหกรรมที่ตื่นตระหนกกับการขาดแคลนธาตุหายากในคลังก็ไม่ต้องกังวลเกี่ยวกับภัยคุกคามที่คล้ายคลึงกันต่อการใช้งานดังกล่าว
ยูโรเพียมออกไซด์ใช้เป็นฟอสเฟอร์กระตุ้นการปล่อยแสงในระบบการวินิจฉัยทางการแพทย์ด้วยรังสีเอกซ์แบบใหม่ ยูโรเพียมออกไซด์ยังใช้ในการผลิตเลนส์สีและตัวกรองออปโตอิเล็กทรอนิกส์ สำหรับอุปกรณ์จัดเก็บฟองแม่เหล็ก และในวัสดุควบคุม วัสดุป้องกัน และวัสดุโครงสร้างของเครื่องปฏิกรณ์อะตอม เนื่องจากอะตอมของยูโรเพียมออกไซด์สามารถดูดซับนิวตรอนได้มากกว่าธาตุอื่น จึงมักใช้เป็นวัสดุสำหรับดูดซับนิวตรอนในเครื่องปฏิกรณ์อะตอม
ในโลกที่ขยายตัวอย่างรวดเร็วในปัจจุบัน การใช้ยูโรเพียมที่เพิ่งค้นพบเมื่อไม่นานมานี้อาจส่งผลกระทบอย่างลึกซึ้งต่อเกษตรกรรม นักวิทยาศาสตร์ได้ค้นพบว่าพลาสติกที่เจือด้วยยูโรเพียมที่มีประจุไฟฟ้าสองขั้วและทองแดงที่มีประจุไฟฟ้าหนึ่งขั้วสามารถเปลี่ยนส่วนอัลตราไวโอเลตของแสงอาทิตย์ให้เป็นแสงที่มองเห็นได้อย่างมีประสิทธิภาพ กระบวนการนี้ค่อนข้างเป็นสีเขียว (เป็นสีเสริมของสีแดง) การใช้พลาสติกประเภทนี้ในการสร้างเรือนกระจกสามารถทำให้พืชดูดซับแสงที่มองเห็นได้มากขึ้นและเพิ่มผลผลิตพืชได้ประมาณ 10%
ยูโรเพียมยังสามารถนำไปประยุกต์ใช้กับชิปหน่วยความจำควอนตัม ซึ่งสามารถจัดเก็บข้อมูลได้อย่างน่าเชื่อถือเป็นเวลาหลายวันในแต่ละครั้ง ซึ่งทำให้สามารถจัดเก็บข้อมูลควอนตัมที่ละเอียดอ่อนในอุปกรณ์ที่คล้ายกับฮาร์ดดิสก์และส่งไปทั่วประเทศได้
เวลาโพสต์: 27 มิ.ย. 2566